En esta sexta y, en principio, última entrada sobre la Radioterapia en tiempos del Coronavirus se aborda un tema que cada vez suscita mayor interés como es el empleo de radioterapia para la mejoría sintomática de los pacientes afectos por neumonía por COVID-19. Al igual que en entradas anteriores se recogieron las publicaciones que hacían referencia a modificaciones propuestas para la radioterapia de distintos tumores durante la pandemia por COVID-19, y que se seguirán actualizando según vayan publicándose nuevos artículos sobre ello, esta última entrada se centra en la posibilidad de emplear un tratamiento tan «antiguo» como la radioterapia contra un atacante tan «nuevo» como SARS-CoV-2.
Todo este interés arranca con la carta que Jerry Cuttler dirige, el 20 de marzo de 2020, a Stephen Hahn, Comisionado de la FDA, apuntando la posibilidad de que una dosis de 0,5 Gy sobre ambos pulmones en fracción única pudiera ser de utilidad frente a la neumonía por COVID-19. El Dr. Cuttler es conocido por su defensa del empleo de dosis bajas de radioterapia para diferentes enfermedades benignas no neoplásicas. A partir de ese momento se desencadena, en analogía con la infección COVID-19, toda una «tormenta de ideas» a través de diferentes redes sociales, incluso creándose de manera espontánea grupos cooperativos internacionales, para buscar la mejor manera de emplear la radioterapia en una enfermedad que, desgraciadamente y hasta ahora, carece de un tratamiento curativo definitivo.

Pese a lo que pudiera parecer, la idea de emplear radioterapia para el tratamiento trastornos respiratorios no es nueva. Existe evidencia, desde los inicios de la radioterapia a finales del siglo XIX y primera mitad del XX, de su utilización y eficacia. Calabrese et al. habían publicado ya distintas revisiones recogiendo los resultados observados con radioterapia para el tratamiento de la tosferina (Radiotherapy for Pertussis: An Historical
Assessment), del asma bronquial (The Use of X Rays in the Treatment of Bronchial Asthma: A Historical Assessment) o de la neumonía (How Radiotherapy Was Historically Used To Treat Pneumonia: Could It Be Useful Today?)
Numerosas son las publicaciones que han analizado, estudiado y planteado las bases teóricas de la utilidad de la radioterapia en COVID-19, al tiempo que han tratado de dar respuesta a los temores y prejuicios, a menudo de poca base, tradicionalmente asociados al empleo de cualquier radioterapia. El interés que ha despertado la posibilidad de emplear radioterapia, un tratamiento de bajo coste y fácilmente accesible sin las restricciones de stock que pueden verse con determinados fármacos, ha trascendido el ámbito meramente científico y ha sido publicado en medios de difusión generalista, como Forbes: How Low-Dose Radiation Could Be The Trick For Treating COVID-19
«As we try lots of possible solutions to rein in the coronavirus SARS-CoV-2, we need to use every tool we have, and low-dose radiation therapy may be an important one. It would be unethical not to investigate this approach as thousands are still dying every day from this pandemic and a vaccine is a long ways off»
Actualmente hay registrados ya 7 estudios abiertos en la plataforma de ensayos clínicos clinicaltrials.gov, incluyendo el ensayo multicéntrico español IPACOVID.
De manera breve, los artículos publicados en estos últimos 60 días son:
Kirkby C, Mackenzie M. Is low dose radiation therapy a potential treatment for COVID-19 pneumonia? [published online ahead of print, 2020 Apr 6]. Radiother Oncol. 2020;S0167-8140(20)30185-7. doi:10.1016/j.radonc.2020.04.004
Este editorial, publicado a principios de Abril de 2020, supuso el inicio del renovado interés en el posible papel de la radioterapia frente al COVID-19. Los autores recordaron los antecedentes históricos, repetidamente invocados y citados desde entonces, sobre la eficacia de las dosis bajas (<100 cGy) para tratar las neumonías. La evidencia histórica apuntaba a la inducción de un fenotipo antiinflamatorio por bajas dosis de radiación como una posible explicación de los efectos observados favoreciendo la disminución de los niveles de citocinas pro-inflamatorias como IL-1β o inhibiendo el reclutamiento de leucocitos. Así, era provocador considerar que un tratamiento con dosis de 0,3-1 Gy en los pulmones de un paciente con neumonía por COVID-19 podría reducir la inflamación y aliviar los síntomas que amenazan la vida. Además, una sola fracción de tratamiento de podría administrarse fácilmente en una unidad convencional de radioterapia de megavoltaje sin alterar el flujo de trabajo habitual. Los autores concluyen afirmando su convencimiento acerca de la necesidad de plantear ensayos clínicos que exploren la opción de la radioterapia pulmonar de baja dosis en la neumonía por COVID-19.
Jamilloux Y, Henry T, Belot A, Viel S, Fauter M, El Jammal T, Walzer T, François B, Sève P, Should we stimulate or suppress immune responses in COVID-19? Cytokine and anti-cytokine interventions, Autoimmunity Reviews, 2020, 102567, https://doi.org/10.1016/j.autrev.2020.102567.
Aunque no hace referencia expresa a la radioterapia a dosis bajas y su posible efecto beneficioso sobre la neumonía por COVID-19, esta excelente revisión debiera ser de obligada lectura antes de plantear siquiera cualquier tratamiento para SARS-CoV-2 ya que explica, de manera clara, sencilla y directa cuál es, cómo es y por qué es la fisiopatogenia de la infección por COVID-19 y todo el cuadro clínico de ello derivado. Los autores explican como una enfermedad que, en la gran mayoría de los casos, era una enfermedad benigna puede también desarrollar una forma grave con resultados a veces fatales.
La inducción de un estado hiperinflamatorio parece ser el mecanismo clave desencadenante de las formas más graves de la infección. Las citocinas juegan un papel determinante en la fisiopatología del COVID-19: mientras que algunas son beneficiosas (interferón tipo I, interleucina-7), otras parecen perjudiciales (interleucina-1β, -6 y TNF-α) particularmente en el contexto de la llamada «tormenta de citocinas». Otra característica de la enfermedad es la aparente inmunodeficiencia concomitante, en particular con la presencia de interferón de respuesta de tipo I deteriorado y linfopenia. En este artículo., los autores presentan los principales hallazgos e intentos de establecer una visión más definitiva de la fisiopatología de COVID-19, enfocados a una pregunta clave: ¿Cómo se puede reforzar la inmunidad antiviral y evitar daños hiperinflamatorios?
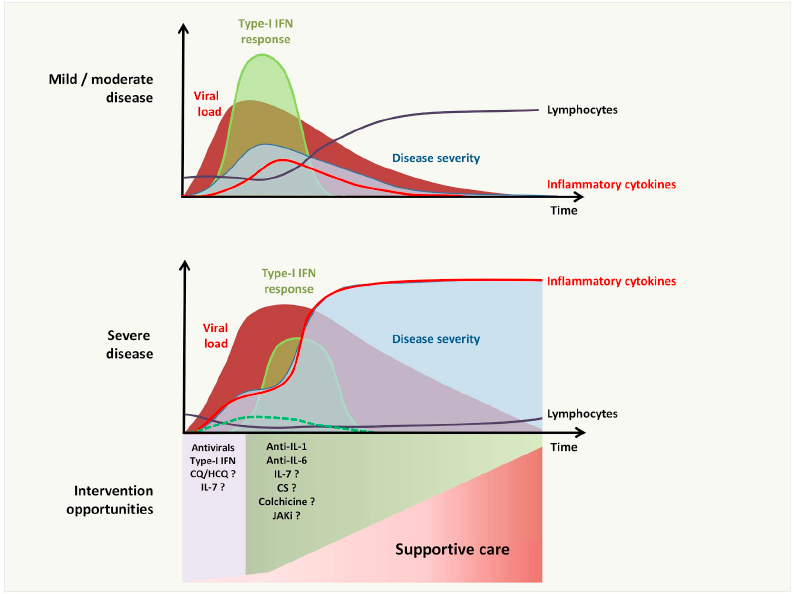
De acuerdo a los datos de los que disponemos actualmente, parecen existir tres fenotipos en pacientes con COVID-19: 1) «Leve» (infección benigna: 80%) en pacientes con síntomas menores e inespecíficos que no progresarán a una enfermedad más grave; 2) «Moderado» (neumonía manifiesta con o sin hipoxia e inflamación localizada: 15%) en pacientes que requieren hospitalización; y 3) «Grave» (hiperinflamación sistémica y SDRS: 5%) en pacientes que requieren manejo en UCI con riesgo de desenlace fatal (1-2%). A pesar de los múltiples intentos, ningún tratamiento ha demostrado ser aún eficaz para la curación definitiva del SARS-CooV-2
La entrada de SARS-CoV-2 en células epiteliales / endoteliales, a través de la unión a ACE2 (y CD147), induce vías apoptóticas y necróticas que resultan en daño pulmonar y liberación de numerosas quimiocinas que impulsan el reclutamiento de grandes cantidades de células inmunes dentro de los pulmones. Las células dendríticas (DC) y DC plasmacitoides (pDC, la fuente principal de interferón tipo I (IFN), junto con los macrófagos y neutrófilos alveolares, promueven la respuesta inmune innata mediante la secreción de alarmas y antivirales o citocinas proinflamatorias, además de presentar el antígeno a las células inmunes adaptativas. El SARS-CoV-2 puede haber desarrollado estrategias para regular negativamente la respuesta mediada por IFN tipo I y capaces de inducir apoptosis de células T. El reconocimiento de patrones moleculares (ARN viral, partículas o señales de peligro) por varios receptores tipo Toll (TLR), receptores tipo NOD (NLR) o receptores similares a RIG-I (RLR) activan la transcripción y la liberación de mediadores proinflamatorios, como la interleucina (IL) -1β, -6, -18 y el factor de necrosis tumoral (TNF) -α. Estos mediadores inducen la transformación de las células T-naive a Th1 o linfocitos citotóxicos (CTL o CD8 +), que a su vez secretan cantidades mayores de citosinas pro-inflamatorias contribuyendo a cera un circulo que conduce a la temida “tormenta de citocinas”, coagulopatía y síndrome de dificultad respiratoria aguda (SDRS).
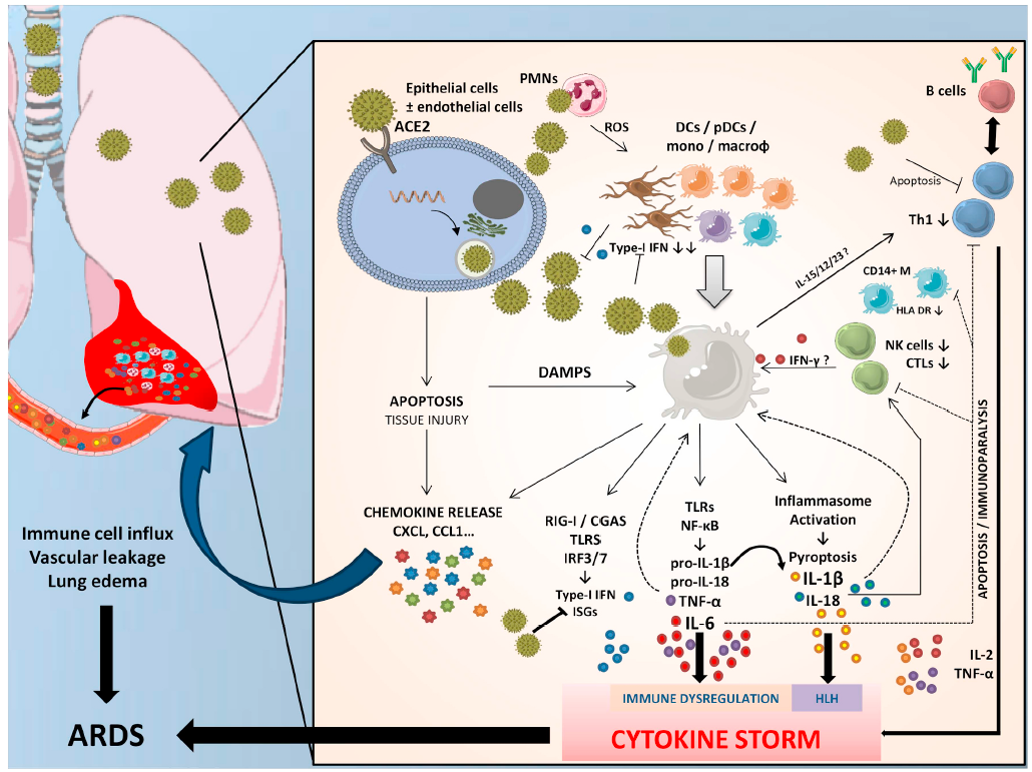
De acuerdo a modelos animales, el retraso en la respuesta mediada por INF tipo I puede explicar una enfermedad más grave, con hiperinflamación. Esto conduce a una afluencia de neutrófilos y monocitos-macrófagos (las principales fuentes de citocinas proinflamatorias) y más apoptosis de células T, células epiteliales y endoteliales. Estos mecanismos inflamatorios agudos dañan el pulmón y su barrera microvascular y alveolar y ocasionan la fuga vascular y edema alveolar, que conduce al establecimiento de SDRS.
En COVID-19 leve o moderado, la respuesta antiviral rápida mediada por INF de tipo I permite la rápida reducción de la carga viral y previene el agotamiento de las células T y la hipercitocinia. En COVID-19 grave, la respuesta retrasada secundaria, entre otras, a la presencia de INF de tipo I deteriorado da como resultado niveles elevados de citocinas / quimiocinas en los pulmones, con deterioro asociado de las respuestas de las células T específicas frente al virus y un consiguiente deterioro clínico agudo.
Mezian L, Robert C, Mordan P, Deutsch E Low doses of radiation therapy increase the immunosuppressive profile of lung macrophages via IL-10 production and IFNγ/IL-6 suppression: a therapeutic strategy to counteract lung inflammation? bioRxiv 2020.05.11.077651; doi: https://doi.org/10.1101/2020.05.11.077651
En este interesante trabajo realizado por investigadores del Institute Gustave Roussy de París intenta explicar las bases que justifican la eficacia de la irradiación pulmonar a dosis bajas con intención antiinflamatoria, y la posible utilidad como tratamiento sintomático de la neumonía COVID-19 severa. Actualmente, no existe un tratamiento curativo para COVID-19. En la mayoría de pacientes con infección por SARS-CoV-2, el tiempo medio de incubación es de 5 días aunque varía de 1 a 14 días. La mayoría de los pacientes presentan infección leve del tracto respiratorio, caracterizado por fiebre (82%) y tos (81%). Sin embargo, en un 14% de los pacientes se ha descrito un síndrome de dificultad respiratoria aguda (SDRS) más grave y la mortalidad global es de alrededor del 1-2%. Los pacientes con COVID-19 grave tienen un marcado estado inflamatorio caracterizado por una «tormenta de citocinas», síndrome, para el cual los agentes antiinflamatorios como el receptor anti-IL-6 tocilizumab y el el antagonista del receptor de IL-1 anakira han demostrado cierta eficacia.
En la fisioptaogenia de la respuesta inflamatoria del pulmón a las infecciones tienen un papel destacado los macrófagos. El pulmón alberga dos poblaciones distintas de macrófagos, macrófagos alveolares (AM) y macrófagos intersticiales (IM). Los MI están ubicados en el intersticio, junto con las células dendríticas y linfocitos Recientemente, se ha descrito también la existencia de una población de macrófagos asociados a las vías respiratorias y nerviosas (NAM) que son distintos de otros subconjuntos de macrófagos residentes en los pulmones y expresan genes inmunorreguladores. Los NAM proliferaron después de infecciones pulmonares víricas, como la gripe, y en su ausencia, la respuesta inflamatoria aumenta dando lugar a una producción excesiva de citocinas inflamatorias e infiltración inmune de células inmunes. Los NAM funcionan para mantener la homeostasis inmune y tisular, y regulan la inflamación inducida por infección a través de la secreción de factores inmunosupresores como la IL-10. La ausencia de NAM durante una infección vírica se caracteriza por la presencia en exceso de citocinas y quimiocinas proinflamatorias como la IL-6, CCL2, CCL3 y CCL5.
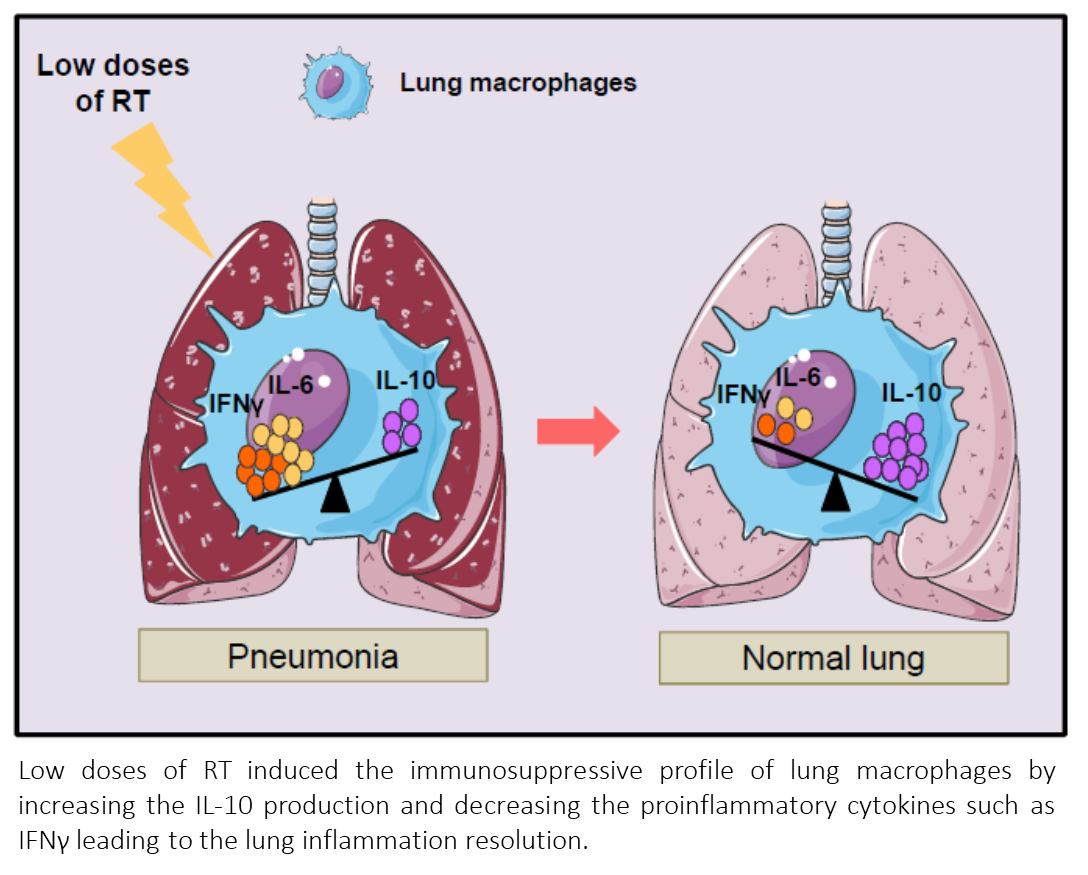
En el estudio realizado por los investigadores en ratones a los que se indujo un estado pro-inflamatorio pulmonar para remedar el producido por una infección vírica grave, la irradiación pulmonar a baja dosis demostró contrarrestar el efecto de los estímulos proinflamatorios in vitro en macrófagos humanos del pulmón; estimular la producción por NAM de citocinas antiinflamatorias IL-10 y proteger los pulmones de los ratones contra la inflamación. Los autores sugieren que la reprogramación de macrófagos de pulmón humano, en particular de la producción de las citocinas inmunosupresoras IL-10 y la supresión de las señales inflamatorias (IL-6 e IFN), podrían ser un mecanismo por el cual bajas dosis de radioterapia protegería el pulmón frente a la neumonía. De este modo, la irradiación torácica de dosis baja única de 0,5-1 Gy podría ser una eficiente estrategia para contrarrestar la inflamación pulmonar severa (SDRS) inducida por COVID-19
Dhawan, G., Kapoor, R., Dhawan, R., Singh, R., Monga, B., Giordano, J., Calabrese, E.J., Low dose radiation therapy as a potential life saving treatment for COVID-19-induced acute respiratory distress syndrome (ARDS), Radiotherapy and Oncology (2020), doi: https://doi.org/10.1016/j.radonc.2020.05.002
La radioterapia se ha empleado desde hace más de un siglo en el tratamiento de neumonías, especialmente intersticiales y atípicas. En la revisión, ya clásica, de Calabrese et al. se evidenció que dosis bajas de irradiación sobre los pulmones se asociaban con buenas tasas de respuesta y resolución de la sintomatología. Los autores revisaron 15 estudios incluyendo 863 casos de neumonía bacteriana (lobular y bronconeumonía), intersticial y neumonía atípica que se trataron eficazmente con dosis bajas de rayos X, mejorando la sintomatología, aumentando la curación y reduciendo la mortalidad. El mecanismo por el cual el tratamiento con rayos X actúa sobre la neumonía implica la inducción de un fenotipo antiinflamatorio que conduce a una rápida reversión de los síntomas clínicos, facilitando la resolución de la enfermedad. El tratamiento era más eficaz cuando la irradiación se administraba antes de 6 a 14 días de la instauración clínica de la enfermedad. Después de 14 días, la tasa de respuesta exitosa se redujo en aproximadamente un 50 por ciento. La conclusión de los autores es que la radioterapia a dosis bajas ofrece un excelente potencial como tratamiento para la neumonía intersticial, especialmente cuando se usa durante las primeras etapas de la enfermedad.
Los fenómenos inflamatorios que el Coronavirus induce en el organismo se manifiestan especialmente en órganos que expresan una alta concentración de enzima convertidora de angiotensina 2 (ACE2), como como corazón, riñones, intestinos y pulmones, con los neumocitos alveolares tipo II de pulmón como objetivo principal. El daño a estos tejidos inicia el sistema renina-angiotensina-aldosterona (RAAS) en cascada e induce inflamación del parénquima pulmonar a través de la actividad de (proinflamatorio) de macrófagos y granulocitos, lo que conduce al desarrollo del SDRS. La «tormenta de citocinas» inducida por linfocitos activados crea una plataforma sistémica para el rápido empeoramiento característico de la enfermedad crítica de COVID-19. Esta respuesta hiperinflamatoria plantea desafíos importantes y se están haciendo esfuerzos para emplear fármacos experimentales (p. ej., inhibidores de citocinas y / o antagonistas de interleucina) que pueden modular eficazmente las respuestas del sistema inmunitario
A diferencia de la radioterapia de dosis alta que induce la producción de citocinas proinflamatorias en las células inmunes y endoteliales, las dosis bajas de radioterapia (0,5-1,5 Gy) actúan sobre las células que participan en la respuesta inflamatoria, produciendo efectos antiinflamatorios. Estos efectos incluyen la inhibición de las interacciones entre los leucocitos y las células endoteliales, una disminución en la producción de moléculas de adhesión al endotelio, una disminución de los mediadores de la inflamación y una menor expresión de citocinas proinflamatorias, además de favorecer la inducción de apoptosis de los macrófagos y polimorfonucleares La irradiación a dosis bajas también produce una disminución en los niveles de NO (óxido nítrico) sintetasa (iNOS), selectinas L y E, especies reactivas de oxígeno (ROS), TNF-α o la secreción de IL-beta 1, junto con un aumento en la producción y expresión de citocinas antiinflamatorias, como el factor de crecimiento transformante de la citocina antiinflamatoria β1 (TGF-β1) y de mediadores de la apoptosis como el factor nuclear kappa-beta (NF-κB). Todos estos cambios resultan en un ambiente antiinflamatorio local que explicaría los efectos clínicos de la radioterapia a dosis bajas.
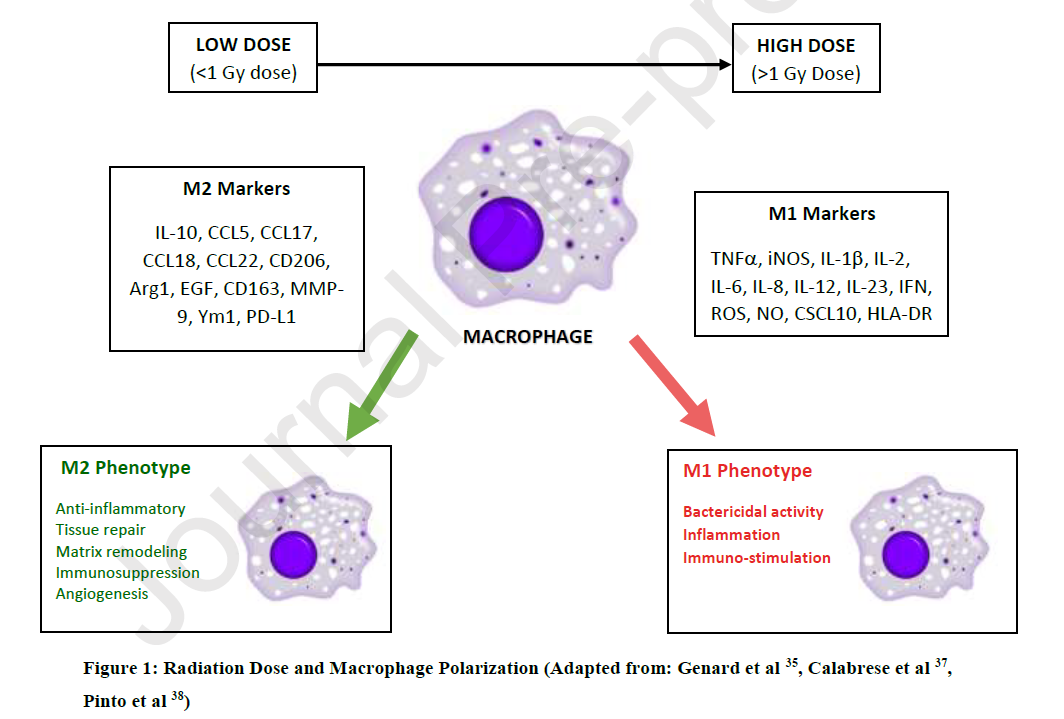
Los autores de esta revisión sugieren que, dadas las limitaciones e insuficiencias actuales en el tratamiento de esta enfermedad, parece pertinente explorar la utilidad y el valor de nuevas modalidades terapéuticas, como la radioterapia de baja dosis. De acuerdo a su experiencia, Dhewan et al. sostienen que dosis bajas de radioterapia inducen una compleja respuesta sistémica que que implica la polarización de los macrófagos a un fenotipo antiinflamatorio M-2 (frente al fenotipo M-1 inducido, por ejemplo, en presencia de infecciones). Este fenotipo antiinflamatorio ocasiona la disminución de la adhesión de leucocitos y células polimorfonucleares (PMN) a las células endoteliales, la disminución de especies reactivas de oxígeno (ROS), la reducción de óxido nítrico (NO), la disminución de la sintetasa de óxido nítrico inducible (iNOS), la disminución del factor de necrosis tumoral alfa (TNF-α) y la disminución del factor de crecimiento tumoral alfa (TGFα). Además de la inducción del fenotipo M2, la radioterapia a dosis bajas induciría un aumento de hemo-oxigenasa, aumento de citocinas antiinflamatorias como interleucina-10 (IL-10), aumento del factor beta de necrosis tumoral (TNF-β), activación de factores de transcripción como el factor nuclear kappa beta (NFkB) y la activación de la proteína-1 (AP-1), aumento del factor de crecimiento tumoral – beta 1 (TGFβ1) 19,20, y mejora de la regulación de los linfocitos T. Finalmente, los autores apuntan a la existencia de una relación directa entre la dosis de radioterapia administrada y el fenotipo inducido en los macrófagos pulmonares, M1 (proinflamatorio) con dosis superiores a 1 Gy frente a fenotipo macrofágico M2 (antiinflamatorio) con dosis inferiores a 1 Gy. Los autores sugieren que la existencia de fenotipos M1 y M2 no son absolutos, sino que existe habitualmente una inducción simultánea de ambos fenotipos pero el potencial fenotípico final (es decir, que determina la constitución relativa de proinflamatorio o fenotipo antiinflamatorio) depende de que la dosis de radiación sea mayor o menor que 1 Gy. La conclusión de los autores es que, teniendo en cuenta la evidencia disponible y el mecanismo de acción propuesto de dosis bajas de radioterapia, una dosis total única de 0,3-0,5 Gy es probable que sea beneficiosa para los pacientes con COVID-19 que presentan síntomas clínicos compatibles con la “tormenta de citocinas”. Además, beneficios añadidos de la radioterapia serían su amplia disponibilidad, bajo coste y no depender de un stock potencialmente agotable.
Rödel, F., Arenas, M., Ott, O.J. et al. Low-dose radiation therapy for COVID-19 pneumopathy: what is the evidence?. Strahlenther Onkol (2020). https://doi.org/10.1007/s00066-020-01635-7
Los autores revisan la evidencia existente acerca de las propiedades antiinflamatorias de la radioterapia a bajas dosis y su posible utilidad en el contexto de la neumonía COVID-19, centrando la discusión aspectos prácticos de gran interés. En primer lugar, existe la certeza de que los máximos efectos antiinflamatorios se producen con dosis entre 0,3 y 0,7 Gy. Por ello, aunque no se dispone de datos experimentales o preclínicos sobre radioterapia de baja dosis en pacientes con COVID-19 que padecen dificultad respiratoria, en analogía con la evidencia mencionada anteriormente, se puede recomendar una dosis única de 0,5 Gy para todo el pulmón con base en la radiobiología y consideraciones clínicas. Además, analiza los posibles riesgos sin olvidar siempre que, en contraste con la mayoría de los enfoques farmacológicos que tienen un efecto sistémico importante en el organismo, la radiación es un tratamiento eminentemente local, con un impacto directo en el órgano afectado por el estrés inflamatorio, es decir, el tejido pulmonar. Las dosis de radiación requeridas para un tratamiento efectivo son muy bajas (<1% de las dosis utilizadas para la radioterapia contra el cáncer) y no exceden las dosis de tolerancia de los órganos críticos en el volumen irradiado, como el corazón, la tiroides, el estómago o los riñones. Generalmente, ser acepta que una exposición de 0,5 Gy no aumenta el riesgo de enfermedad cardíaca, aunque algunos estudios apuntan un mayor riesgo de enfermedad circulatoria y sufrimiento cardíaco isquémico incluso a dosis inferiores a 0,5 Gy. Sin embargo, y como recalcan los autores de esta revisión, salvar vidas en la situación actual es el factor más importante y puede justificar el tratamiento por irradiación.
Otro aspecto clave es determinar el momento adecuado de la irradiación. En las etapas crónicas de la enfermedad caracterizada por el síndrome de liberación de citocinas (“tormenta de citocinas”), la irradiación a dosis bajas puede no ser tan eficiente como en la etapa más temprana. El momento de la irradiación debe elegirse cuidadosamente para evitar la atenuación de la respuesta inmune que resuelve la enfermedad, por ejemplo, estimulando los IFN-I. La indicación de dosis bajas de radioterapia debe basarse en la función pulmonar, es decir, la progresión de la dificultad respiratoria.
Finalmente, otro punto a considerar es que se espera que las dosis bajas de irradiación en los pulmones infectados, incluso a dosis de hasta 0,5 Gy, induzcan un bajo número de eventos de daño al ARN y mutaciones en el virus, aunque no debe obviarse que cualquier tratamiento con medicamentos antivirales contra el SARS-CoV-2 probablemente resultaría en una presión selectiva más intensa sobre el virus.
Dörthe Schaue & William H. McBride (2020): Flying by the Seat of our Pants -Is low Dose Radiation Therapy for COVID-19 an Option?-, International Journal of Radiation Biology, DOI: 10.1080/09553002.2020.1767314
Los autores realizan una amplia y concienzuda revisión de la utilidad de la radioterapia como tratamiento antiinflamatorio en diferentes patologías no tumorales y plantean la hipótesis de una posible utilidad en el seno de la pandemia COVID-19, sin perder no obstante de vista el hecho de que la gran mayoría de los pacientes evolucionan bien sin intervención médica y que una serie de otros antiinflamatorios y antivirales están ya disponibles.
Los autores analizan las primeras evidencias de principios del siglo XX y como las dosis bajas, en el rango de 0,3 – 3 Gy, eran empleadas de acuerdo a Ley de la modulación de Arndt-Schultze que establece que las dosis mínimas estimulan, las dosis medias inhiben o suprimen, y las dosis altas destruyen la actividad celular. Además, desde el principio se estableció que la eficacia en la irradiación de diversas enfermedades agudas era mejor si la radiación se administraba de manera temprana
Una posible ventaja de la radioterapia a bajas dosis sería que actúa interfiriendo potencialmente con varios procesos inflamatorios y pro-oxidantes a múltiples niveles, mucho más de lo que las drogas dirigidas a una sola citocina podrían hacer. Sin embargo, los autores también plantean sus dudas acerca de la manera más correcta de identificar a los pacientes con mayor probabilidad de beneficiarse del tratamiento con radiación, e identificarlos lo suficientemente temprano como para tener el impacto deseado.
Finalmente, los autores plantean 6 cuestiones a resolver para considerar la radioterapia a bajas dosis como tratamiento en neumonía COVID-19:
- ¿Cuáles son los indicadores de que un paciente con COVID-19 se deteriore rápidamente: carga viral, edad, género, peso, perfiles leucocitarios circulantes, marcadores inflamatorios sistémicos, niveles de dímero D, niveles, medio ambiente, carga genética?
- ¿Qué condiciones preexistentes predicen la susceptibilidad y la mortalidad? ¿Cómo se definen estos? ¿Cómo se relacionan con la inflamación y los cambios redox inducidos por la enfermedad?
- ¿La COVID-19 tiene patrones de enfermedad distintos en subgrupos de pacientes en fases clínicas diferentes y eso podría dictar la elección del tratamiento? En otras palabras: ¿todos los pacientes que enfermarse gravemente y sucumbir a la enfermedad, todos fallan de la misma manera?
- ¿Existen características genéticas que se correlacionan con la susceptibilidad y la mortalidad de COVID-19 que indicaría mecanismos de patogenicidad difere?
- ¿Cuál es el principal mecanismo de la patología pulmonar COVID-19? ¿Está esto predominantemente controlado por células mieloides o linfoides?¿Cómo funciona el perfil de citocinas, local y sistemáticamente? ¿Cambia con el tiempo después de la infección y la etapa de la enfermedad? ¿Cuál es la incidencia y composición de cualquier «tormenta de citocinas» y su papel en la enfermedad? ¿Cuál es el papel de la linfopenia y cuál es el mecanismo de su inducción? ¿La linfopenia puede ser exacerbada por la irradiación a dosis bajas?
- ¿En qué pacientes se debe usar la radioterapia? ¿Cuándo debería comenzar, con qué dosis, con qué frecuencia y con qué volumen / tamaño de campo?
Cosset JM, Deutsch É, Bazire L, Mazeron JJ, Chargari C. Irradiation pulmonaire à faible dose pour l’orage de cytokines du COVID-19 : pourquoi pas ? [Low dose lung radiotherapy for COVID-19-related cytokine storm syndrome: Why not?]. Cancer Radiother. 2020 May 1. pii: S1278-3218(20)30099-8. doi: 10.1016/j.canrad.2020.04.003.
Los autores de este trabajo apuntan a un aspecto muy interesante en la utilización de dosis bajas de radioterapia como es la posibilidad, conocida desde antiguo, de inducir linfopenia por la irradiación. Parece contra toda lógica intentar favorecer un estado inmunocomprometido ante una infección, aunque es cierto que no se ha visto especial virulencia del COVID-19 en pacientes de por sí inmunosuprimidos, y no se recomienda, por ejemplo, suspender el tratamiento inmunosupresor en estos pacientes. De hecho, y como apuntan resultados de estudios chinos e italianos, «los pacientes con inmunosupresores podrían tener un menor riesgo de desarrollar formas graves de COVID-19».
Por otro lado, un porcentaje importante de pacientes tratados con radioterapia por distintos cánceres van a recibir una dosis baja en los pulmones como consecuencia de la irradiación dispersa, que están en el rango de 0,3-1 Gy, y que no parecen tener trascendencia negativa. Del mismo modo, la irradiación abdomino-pélvica con campos amplios también induce linfopenia secundaria a la irradiación del tejido esplénico. ¿Podría esta linfopenia ser “protectora” frente a las formas más graves de COVID-19? Los autores proponen que sería interesante conocer el comportamiento de estos pacientes frente a SARS-CoV-2.
Finalmente, los autores recuerdan que, a día de hoy, no existe tratamiento curativo definitivo, por lo que considerar la irradiación pulmonar a dosis bajas con estas premisas no parece nada descabellado. Además de la linfopenia “protectora” secundaria, estudios recientes sugieren redistribuciones dinámicas de poblaciones macrofágicas después de la irradiación pulmonar (macrófagos alveolares, macrófagos intersticiales), estas observaciones pueden tener aplicaciones en la comprensión de la fisiopatología de COVID-19, así como en el desarrollo de agentes farmacológicos dirigidos a la activación macrofágica. Por tanto, este tipo de tratamiento podría proponerse para las formas pulmonares graves de COVID-19, en particular las asociadas con imágenes de TC difusas, con la posibilidad añadida de poder evaluar rápidamente mediante imágenes radiológicas la efectividad (o no) de estas bajas dosis de irradiación.
Sisko Salomaa, Elisabeth Cardis, Simon D. Bouffler, Michael J. Atkinson & Nobuyuki Hamada (2020): Low dose radiation therapy for COVID-19 pneumonia: is there any supportive evidence?, International Journal of Radiation Biology https://doi.org/10.1080/09553002.2020.1762020
Los autores de esta revisión, todos ellos dedicados a la epidemiología y estudio de la protección radiológica, intentan analizar desde un punto de vista crítico, la posibilidad de emplear radioterapia a bajas dosis con intención antiinflamatorioa en la actual pandemia por COVID-19. Los autores de este trabajo repasan inicialmente las posibles evidencias existentes acerca de un efecto antiinflamatorio de la irradiación pulmonar a bajas dosis haciendo especial hincapié en la revisión de Calabrese y Dhawan (2013) que incluye 19 artículos que describen los resultados de dosis bajas de radioterapia neumonía publicados entre 1905 y 1943. De acuerdo a lo recogido en esta revisión, de un total de 863 casos de neumonía de distintas causas que recibieron radioterapia pulmonar, 717 mostraron buena respuesta clínica dentro de los tres primeros días tras el tratamiento. No obstante, Salomaa et al. inciden en el hecho de que, de acuerdo al Comité Científico de las Naciones Unidas sobre los Efectos de la Radiación Atómica (UNSCEAR 2008), estudios basados en los datos de los supervivientes de la bomba atómica japonesa, las dosis pulmonares de 0,3-1 Gy inducirían nominalmente un exceso de entre 0,6–4.4 cánceres de pulmón por cada 100 personas expuestas, al igual que, de acuerdo a los mismos análisis, las dosis que recibirían en estos casos tanto aorta como corazón asociarían un riesgo de 0,8–7,6 muertes adicionales por enfermedad circulatoria por cada 100 personas expuestas. El hecho de que, peses a la amplia experiencia existente en el empleo de irradiación a dosis bajas con intención antiinflamatoria – no está de más recordar que en Alemania este tipo de radioterapia representa entre 10%-30% de la carga de trabajo diaria en los Servicios de Oncología Radioterápica – no se hayan confirmado, después de muchos años de seguimiento, tan negros augurios se justifica, en opinión de los autores, en que a diferencia de los sitios tratados por para afecciones inflamatorias benignas, el pulmón es radiosensible, y el edema inducido por radiación, la neumonitis y la fibrosis están bien documentadas. Para ello, los autores acuden a estudios realizados tras tratamientos de cáncer de mama, cáncer de pulmón o Enfermedad de Hodgkin, olvidando (¿intencionadamente?) las diferencias existentes en dosis total, dosis/fracción, duración total del tratamiento, tratamientos sistémicos asociados, etc.
Los autores concluyen afirmando que, en general, la evidencia existente sobre los efectos antiinflamatorios frente a proinflamatorios a dosis muy bajas no son claros, y que, probablemente, exista más bien un equilibrio entre los dos tipos de efecto que resta evidencia y utilidad al empleo de radioterapia a bajas dosis en la neumonía por COVID-19 o que niegan que ésta pudiera ser superior a cualquiera de los potenciales agentes terapéuticos actualmente en ensayos clínicos. Ensayos que, bueno es recordarlo, no han demostrado, hasta la fecha, ser de extraordinaria utilidad y, antes bien, sus resultados (pobres) han sido puestos en entredicho y criticada la calidad y metodología de los mismos. Sin embargo, a juicio de los autores, no existiría justificación para plantear ensayos clínicos sobre el empleo de radioterapia pulmonar a bajas dosis en este momento.
Kirsch, D.G., Diehn, M., Cucinoata, F.A., Weichselbaum, R., Lack of supporting data make the risks of a clinical trial of radiation therapy as a treatment for COVID-19 pneumonia unacceptable, Radiotherapy and Oncology (2020), doi:https://doi.org/10.1016/j.radonc.2020.04.060
Los autores de esta revisión reconocen el impacto terrible de la pandemia por COVID-19 así como la angustiosa situación de no disponer de tratamientos específicos eficaces pero justifican su oposición al empleo de radioterapia pulmonar a baja dosis propuesta por diferentes grupos de distintos países en 4 aspectos que consideran relevantes:
a) Lo anecdótico de los datos existentes acerca de la eficacia de la radioterapia a bajas dosis en el tratamiento de la neumonía (estudios antiguos, técnicas desconocidas, seguimientos inciertos, etc)
b) La eficacia mínima o nula evidenciada en modelos preclínicos que, al igual que sucede con los datos sobre pacientes, se basan en estudios antiguos de diseño discutible, etc.
c) Los riesgos existentes asociados el empleo de irradiación del tórax, aún a bajas dosis
d) Los riesgos asociados que para el personal profesional de los Servicios de Oncología Radioterápica supondría tratar pacientes con infección COVID.-19 (quizás este último punto se comenté por si sólo cuando los autores anteponen la salud personal al ejercicio de la Medicina, y cuando existen mecanismos y protocolos para minimizar los riesgos, y cuando otros profesionales tratan a diario pacientes COVID-19 sin pretender justificar una negativa a hacerlo basada en “miedos personales al contagio”,…, sólo quizás)
Probablemente, este último punto que contradice todo lo que los médicos y demás profesionales de la Medicina hemos asumido como un hecho inherente a nuestra profesión desde hace milenios, anteponer la salud del enfermo por delante incluso de la vida propia, serviría para desestimar las conclusiones de este artículo. Aun así, conviene seguir leyéndolo para encontrar una justificación a la oposición de estos estudios en el potencial riesgo de tumores inducidos por la irradiación a dosis bajas, especialmente en pacientes jóvenes y basados en estudios teóricos pero que los autores parecen aceptar y asumir como verdaderos sin atisbo alguno de crítica. Kirsch et al. sostienen que los ensayos clínicos de radioterapia para COVID-19 solo deben iniciarse después de que resultados sólidos en modelos preclínicos demuestran eficacia. Quizás los autores desconocen que la mayoría de estudios en marcha de radioterapia pulmonar a baja dosis en COVID-19 indican el tratamiento precisamente para personas de más edad, en los que no exista indicación de medidas agresivas de ventilación IOT por edad avanzada y/o comorbilidades, y en los que el riesgo potencial de tumores radio-inducidos a 20-30 años quizás no sea su principal problema.
Kefayat A, Ghahremani F. Low dose radiation therapy for COVID-19 pneumonia: A double-edged sword [published online ahead of print, 2020 Apr 20]. Radiother Oncol. 2020;S0167-8140(20)30207-3. doi:10.1016/j.radonc.2020.04.026
Siguiendo el ejemplo de otros grupos, los autores plantean en esta carta una serie de dudas acerca de la utilidad y eficacia de la radioterapia a bajas dosis en el tratamiento de la neumonía por COVID-19. En primer lugar, la evidencia que lo sostiene es antigua, basada en series de casos y con limitaciones en los estudios que las hacen poco compatibles con los estándares actuales de evidencia basada en grandes estudios aleatorizados y controlados. En segundo lugar, la radioterapia a dosis bajas se emplea actualmente para el alivio sintomático de trastornos inflamatorios musculo-esqueléticos, y es posible que la “tormenta de citocinas” asociada a la neumonía por COVID-19 no responda de la misma manera que lo hacen artritis o tendinitis. En tercer lugar, el momento de la administración del tratamiento antiinflamatorio es muy importante. Los casos fatales de COVID-19 son, generalmente, muy rápidos y se deterioran en menos de dos semanas tras el inicio. Por lo tanto, administrar la radioterapia antes de este deterioro parece fundamental para poder optimizar su resultado. Finalmente, algunos estudios han informado sobre el aumento significativo de la captación, activación, transcripción y propagación de algunos virus después de la radioterapia por lo que, de acuerdo a los autores, tal vez sería más adecuado no utilizar los pulmones como órgano diana para la radioterapia debido a su alta concentración de virus, debiendo considerarse volúmenes blancos de irradiación alternativos
Chakrabarti D, Verma M. Low-dose radiotherapy for SARS-CoV-2 pneumonia [published online ahead of print, 2020 May 11]. Strahlenther Onkol. 2020;1‐2. doi:10.1007/s00066-020-01634-8
Los autores reconocen que, si bien la mayor parte de nuestro conocimiento sobre el uso de la radiación X para tratar la neumonía proviene de informes de casos y series de casos publicados hace más de medio siglo que no cuentan como evidencia sólida en la actualidad, las perspectivas parecen prometedoras en las circunstancias actuales Una sola fracción de radioterapia de dosis baja es coste-efectiva y podría aliviar los síntomas de dificultad respiratoria rápidamente, ayudando a reducir la mortalidad y sin secuelas significativas a largo plazo. Esto, a su vez, facilita el alta temprana del hospital y reduce los costes de hospitalización, lo que finalmente conduce a una mejor utilización de los recursos ante una emergencia global. Los autores plantean que profundizar en esta línea debe considerarse y que necesita de la cooperación internacional y la evaluación rápida en un ensayo controlado y aleatorizado. Como concluyen los autores, ante una pandemia que se originó en Hubei (China), deberíamos recurrir al filósofo chino Confucio en busca de palabras de sabiduría: «Estudia el pasado si quieres conocer el futuro». El pasado pues, puede tener la llave (o una de ellas) para ayudar al alivio de esta pandemia.
Lara PC, Burgos J, Macias D. Low dose lung radiotherapy for COVID-19 pneumonia. The rationale for a cost-effective anti-inflammatory treatment. Clin Transl Radiat Oncol. 2020;23:27‐29. Published 2020 Apr 25. doi:10.1016/j.ctro.2020.04.006
En esta revisión, los autores recuerdan la relación existente entre el SDRS asociado a la neumonía COVID-19 y la “tormenta de citocinas” desencadenada tras la infección por coronavirus. En la misma línea de Dhawan et al., los autores sugieren que este subconjunto de macrófagos M1 «proinflamatorio» es activado por microorganismos infecciosos (por los lipopolisacáridos) y citocinas (interferón-γ). Los macrófagos M1 participan en el inicio y desarrollo de eventos inflamatorios, a través de la liberación de citocinas inflamatorias como IL-1β, IL-6 y TNF-α. La activación continua y no controlada de los macrófagos M1 puede causar daño tisular responsable del rápido deterioro clínico de los pacientes. Las dosis bajas de radioterapia (0,5 Gy) pueden ser de utilidad en este contexto ya que pueden provocar la polarización de los macrófagos a los macrófagos activados alternativamente (fenotipo M2). Los macrófagos M2 «antiinflamatorios» expresan altos niveles de citocinas antiinflamatorias. En la actualidad, la evidencia disponible sugiere que los desequilibrios M1 / M2, que favorecen el fenotipo M1, se encuentran en la patogénesis de la artritis reumatoide y posiblemente en la neumonía relacionada con IL-6 SARS-CoV-2. Y es este conocimiento el que justifica el empleo de medicación frente a la artritis reumatoide en el contexto de la neumonía por COVID-19. Así,
Tocilizumab es un anticuerpo monoclonal contra el receptor de IL-6 humano aprobado para el tratamiento de la artritis reumatoide y que también es eficaz en el tratamiento de pacientes con síndrome de liberación de citocinas grave causados por la terapia CAR-T. Su mecanismo de acción justifica su empleo en pacientes con SARS-CoV-2 con “tormenta de citocinas” buscando el bloqueo de IL-6 . Sin embargo, su disponibilidad plantea problemas de uso en todos los casos de neumonía COVID-19, habiéndose establecido unos criterios restrictivos para el uso de tocilizumab y la derivación a Unidades de Cuidados Intensivos (UCI) durante esta pandemia de COVID-19, debido a la escasez de equipos de respiración asistida y al acceso al tratamiento con tocilizumab. Por ello, los autores sugieren considerar nuevos enfoques para el tratamiento de esta neumonía por COVID-19
La radioterapia de baja dosis (0,5 Gy), es un tratamiento antiinflamatorio basado en la evidencia, que podría modificar el paisaje inmune en el pulmón afectado por la neumonía por COVID-19. Estudios recientes indican que las dosis bajas de radioterapia polarizan los macrófagos hacia un fenotipo similar a M2 en un modelo de artritis reumatoide. En este estudio, una dosis única de 0,5 Gy influyó en el equilibrio M1 / M2 hacia el fenotipo «antiinflamatorio» M2 cuando los sinoviocitos, similares a fibroblastos y los macrófagos derivados de la médula ósea, se cultivaron conjuntamente en un modelo experimental de artritis reumatoide. Por lo tanto, la radioterapia a dosis bajas podría tener un papel relevante en aquellas situaciones en las que la hiperinflamación se asemeja a la artritis reumatoide y contribuyendo a la reducción en la expresión de IL-6. La única limitación para el uso de radioterapia a dosis bajas como un tratamiento antiinflamatorio es el temor a las enfermedades inducidas por la radiación a largo plazo, especialmente el cáncer. Sin embargo, muchos de los «tratamientos estándar» considerados (AINE, inhibidores de la COX, esteroides, tocilizumab, etc.) también tienen efectos secundarios que deben sopesarse, especialmente en pacientes ya afectados por comorbilidades o edad avanzada, frente al muy pequeño riesgo de carcinogénesis. La mayor evidencia de cáncer inducido por radiación proviene de exposiciones accidentales de la población general. El modelo lineal sin umbral (LNT) desarrollado a partir de tales exposiciones accidentales, puede sobrestimar los riesgos en un orden de magnitud. Por lo tanto, no puede ser útil para estimar el riesgo de cáncer mediante el uso de radioterapia a bajas dosis para enfermedades no malignas. Además. La edad es fundamental cuando se estima el riesgo de cáncer inducido por la radiación ya que, por la larga latencia esperada para el desarrollo de tumores, el riesgo de inducir cáncer sería aún menor en pacientes mayores de 40 años. En la amplia experiencia existente con el empleo de radioterapia a dosis bajas en otras enfermedades no neoplásicas no se demostrado un mayor riesgo de cáncer con radioterapia a dosis bajas.
Finalmente, los autores subrayan que la radioterapia a dosis bajas es un tratamiento no tóxico, muy rentable y que ya está disponible en la mayoría de los hospitales generales. Este hecho permitiría su empleo en gran cantidad de pacientes que sufrirán esta enfermedad, y que no recibirían tratamientos específicos anti-IL-6 en UCI en países de bajos y medianos ingresos.
Ghadimi-Moghadam A, Haghani M, Bevelacqua JJ, Jafarzadeh A, Kaveh-Ahangar A, Mortazavi SMJ, Ghadimi-Moghadam A, Mor- tazavi SAR. COVID-19 Tragic Pandemic: Concerns over Unintentional “Directed Accelerated Evolution” of Novel Coronavirus (SARS-CoV-2) and Introducing a Modified Treatment Method for ARDS. J Biomed Phys Eng. 2020;10(2):241-246. doi: 10.31661/jbpe.v0i0.2003-1085.
Los autores de esta propuesta de tratamiento son investigadores de Irán, uno de los países más afectados por la pandemia por SARS-CoV-2. Los autores revisan la epidemiología de la infección y las características de la neumonía asociada, que son bastante inespecíficos, desde neumonía completamente asintomática hasta neumonía grave y muerte. Entre los pacientes con COVID-19, aproximadamente el 80% de los pacientes confirmados por laboratorio mostraron enfermedad leve a moderada.
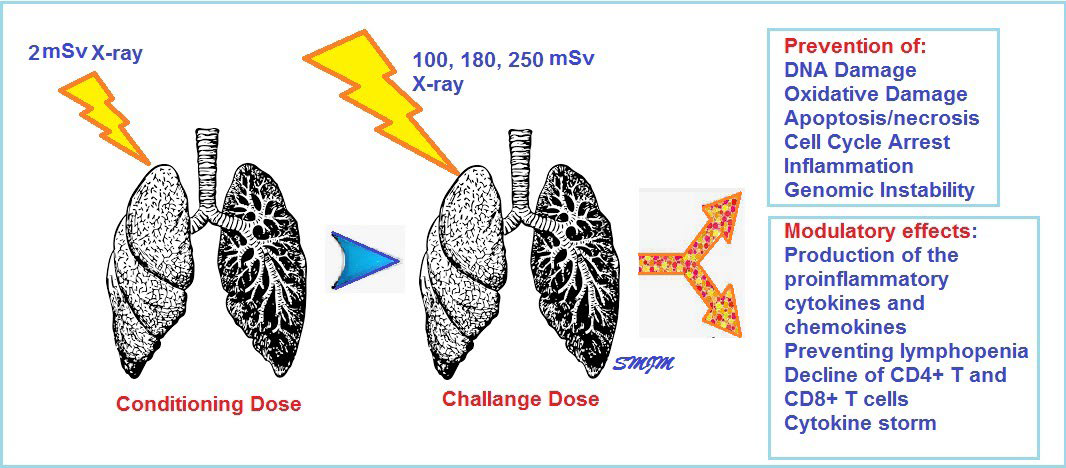
En la situación actual, y el quebranto que la neumonía por COVID-19 está produciendo en los sistemas de salud, se hace necesario poder ofrecer alternativas válidas para intentar afrontar la pandemia. Desde esta perspectiva, los autores plantean un protocolo para manejar la neumonía en pacientes con COVID-19 basado en el empleo de dosis muy bajas de radioterapia. En este protocolo, los pacientes los pacientes recibirán una dosis única de inducción (unos pocos mSv de rayos X) seguido de una dosis única de radiación con rayos X de 100, 180 o 250 mSv, que es menor que la dosis de radiación anual máxima de los residentes de las áreas con “alta” radiación de fondo de Ramsar que es de hasta 260 mSv. El objetivo es aprovechar las ventajas de las bajas dosis de radioterapia (efectos moduladores en la producción de citocinas y quimiocinas proinflamatorias, prevenir la linfopenia, prevenir la disminución de las células T CD4 + T y CD8 + y la posible modulación de la linfopenia y la “tormenta de citocinas” en pacientes con COVID-19), sin aumentar el riesgo potencial de estas dosis terapéutica de rayos X.
Montero A, Arenas M, Algara M. Low‑dose radiation therapy: could it be a game‑changer for COVID‑19? Clinical and Translational Oncology 2020, Vol.:(0123456789)1 https://doi.org/10.1007/s12094-020-02401-y
En una situación desconocida en prácticamente todo su comportamiento, haciendo frente a una infección contra la que no existe tratamiento definitivo curativo, muchas son las alternativas que se han propuesto, y que continúan proponiéndose. Cuando el panorama comienza a aclararse, y tratamientos aceptados como «estándares» y empleados de manera profusa en el convencimiento de su eficacia empiezan a demostrar su escasa o nula eficacia – como ha sucedido recientemente con la hidroxicloroquina – o cuando los «nuevos» (y enormemente costosos) fármacos no terminan de demostrar su utilidad – remdesivir – quizás es el momento de considerar un tratamiento antiguo, modesto (por lo barato y no estar sometido a las fluctuaciones del mercado), aparentemente poco sexy y plagado de (infundados) prejuicios como la radioterapia y reconocer que puede, en todo este marasmo en el que nos movemos, tener un papel eficaz, efectivo y eficiente frente a la neumonía por SARS-CoV-2. Quizás ha llegado ya el momento de sacudirnos todos los complejos, abandonar ideas preconcebidas y ofrecer todo lo bueno que la radioterapia puede conseguir, también frente al COVID-19.
«It is only afterwards that a new idea seems reasonable.
To begin with, it usually seems unreasonable»
Isaac Asimov, bióquimico y escritor estadounidense (1920-1992)